近日,云南大学附属医院(第一通讯单位)杨莹团队联合上海交通大学医学院附属瑞金医院崔文国及杨克团队在Advanced Science(IF=14.3,JCR Q1)期刊发表了题为 Decursin-Loaded Nanovesicles Target Macrophages Driven by the Pathological Process of Atherosclerosis的研究论文,云南大学附属医院陈辉硕士为文章第一作者。

该研究成功开发全球首款基于传统中药成分的动脉粥样硬化靶向纳米递送系统ALD@EM。这项技术的突破,标志着我国在心血管疾病精准治疗领域实现重大跨越,为全球动脉硬化患者带来曙光。
动脉粥样硬化(Atherosclerosis, AS)是威胁人类血管健康的首要“杀手”,亦是心肌梗死、脑卒中等严重心脑血管事件的根本病因。其发生发展可归结为脂质代谢紊乱所触发的病理级联:血浆低密度脂蛋白(LDL)在动脉壁内沉积并经氧化修饰,吸引单核——巨噬细胞浸润,巨噬细胞吞噬过量脂质后转化为泡沫细胞,进而释放炎症介质,使局部内皮功能障碍与脂质沉积进一步恶化,形成“脂质沉积——炎症放大”的恶性循环。现有治疗手段虽可部分干预相关环节,却难以精准扭转病灶核心,且副作用不容忽视:传统他汀类药物在有效降脂的同时,临床上可诱发新发糖尿病,发生率高达约12%;而新兴的抗炎单克隆抗体治疗虽能抑制炎症,却伴随显著感染风险。鉴于此,研发兼具安全性、靶向性与高效性的创新治疗策略已迫在眉睫,以期真正切断动脉粥样硬化的病理循环并降低相关事件的总体发生率。
“三层导航”纳米囊泡-ALD@EM,让药物会“自己找路”
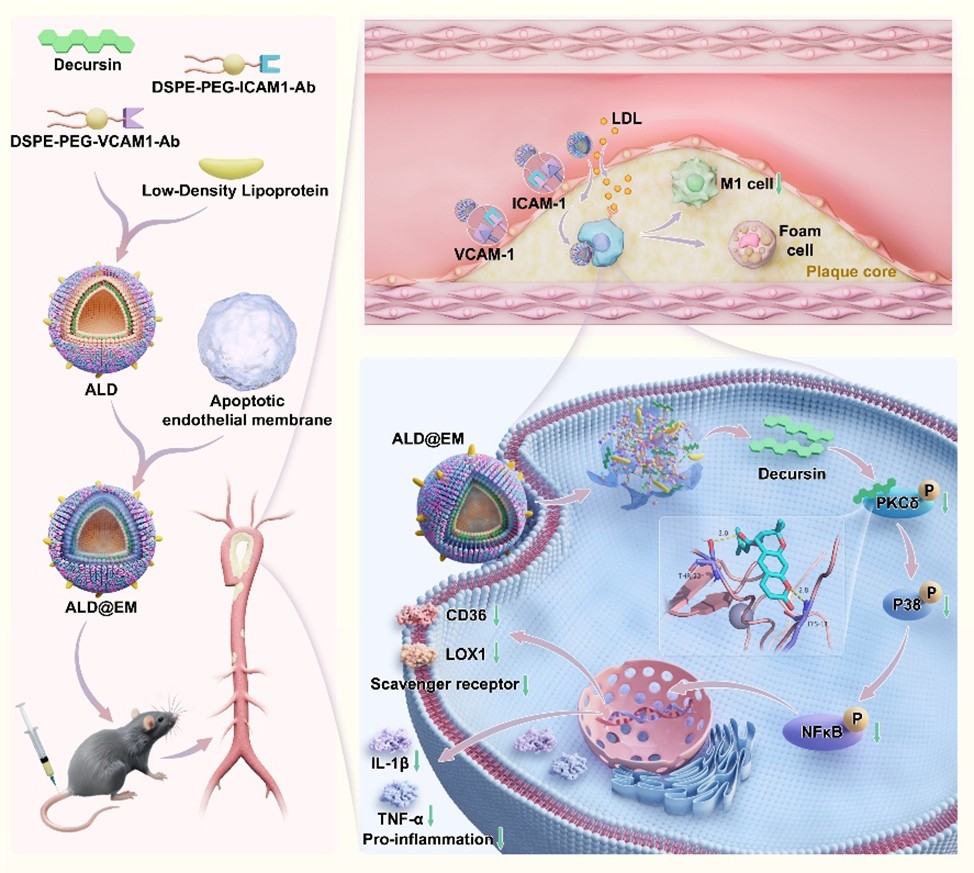
研究团队将目光投向传统中医药宝库,从中药当归(Angelica gigas Nakai)的根部提取出一种活性单体——Decursin。初步研究令人振奋:Decursin在体外实验中显示出强大的潜力,它能够直接抑制巨噬细胞吞噬脂质和减轻炎症反应,并且细胞毒性很低,在动物实验中也表现出良好的安全性。这表明,Decursin有望成为对抗动脉粥样硬化的“天然武器”。然而, Decursin生物利用度低(在体内真正能被吸收利用的比例不高),且在血液中停留的时间很短(半衰期短),很容易在到达血管深处的病灶前就被分解代谢掉,这极大地限制了它的临床应用潜力。
团队首创“瀑布式”靶向设计,将纳米囊泡外层插入 ICAM-1 与 VCAM-1 抗体,帮助其在血流中先锁定受损内皮;中层包埋 LDL 颗粒,借助动脉斑块对胆固醇的“化学趋肤”倒流至核心;最内层披覆凋亡内皮细胞膜,激活巨噬细胞“吃掉”囊泡并瞬时释放Decursin。三套导航环环相扣,让药物有效浓度在斑块处放大数十倍。
传统智慧的现代启示:潜力无限的Decursin
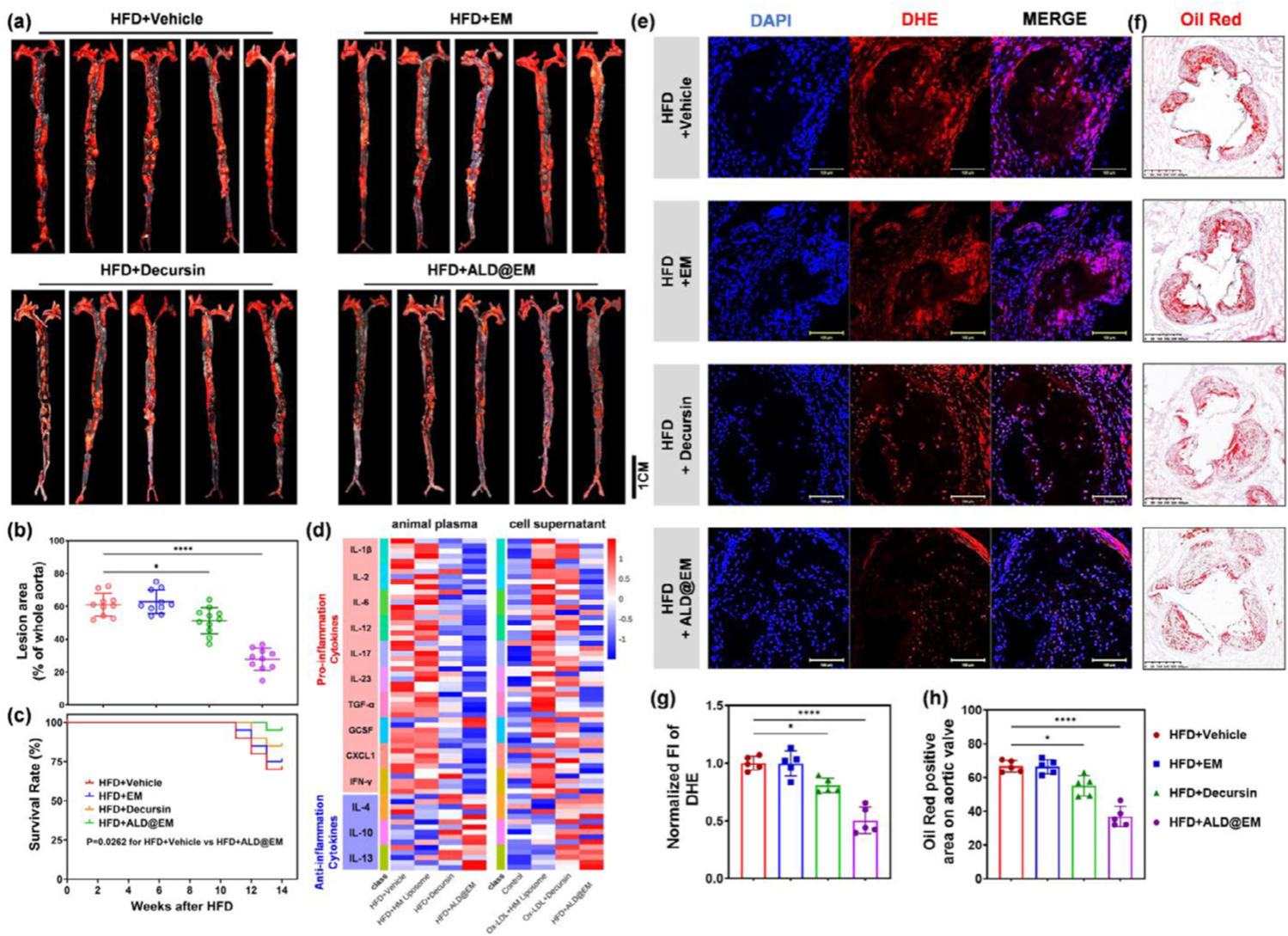
在为期14周的动物实验中,ALD@EM治疗组展现出惊人效果:1)主动脉斑块面积减少45.6%(对照组仅10%);2)炎症因子TNF-α水平下降61%;3)心功能指标EF值提升28%;4)肝肾毒性零报告,为未来慢病管理奠定安全基石。
Decursin结合新靶点蛋白机制揭秘
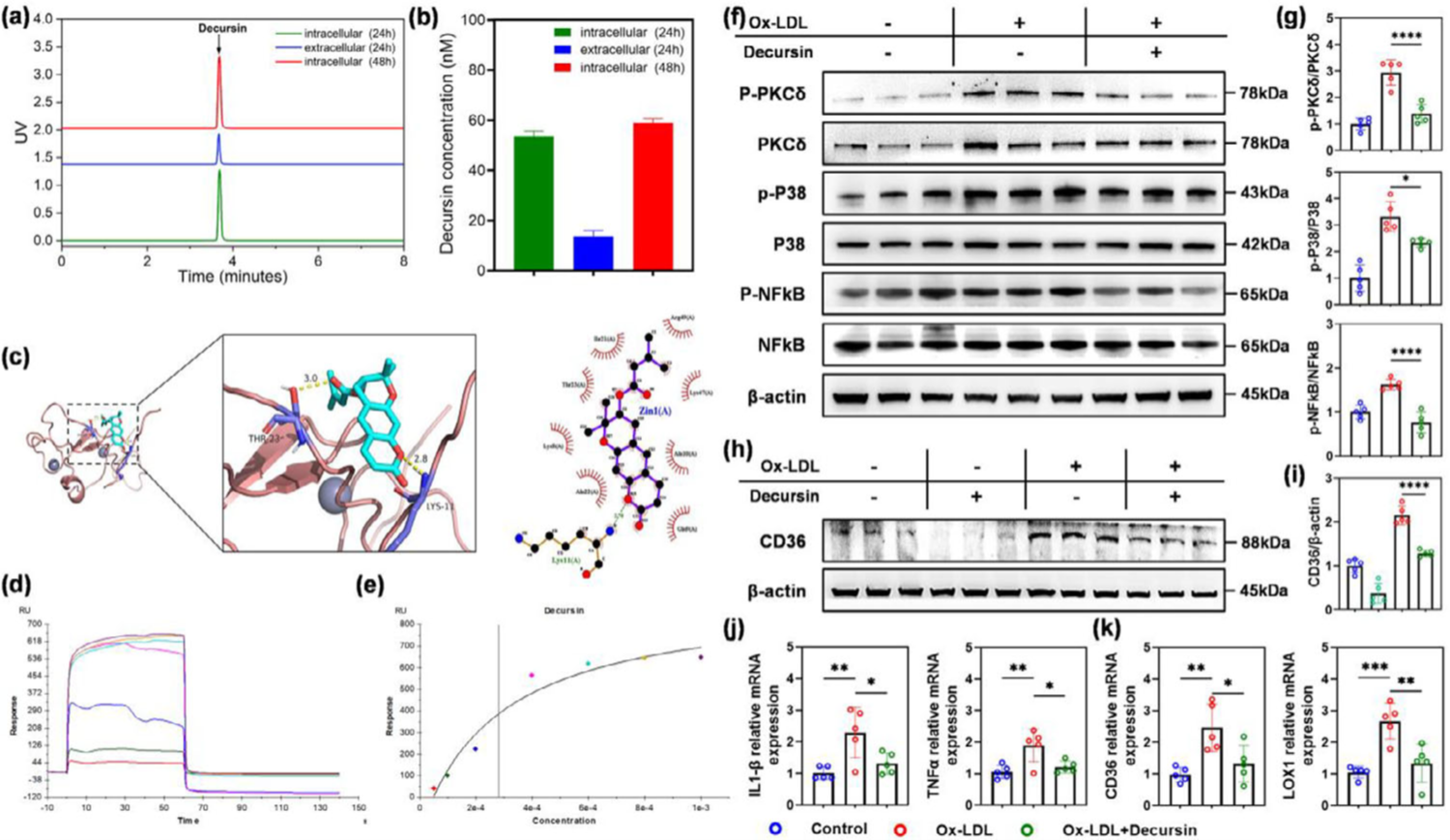
团队通过多种研究手段,首次证明Decursin通过进入细胞发挥药物活性,而其中PKCδ作为炎症反应传递的重要蛋白激酶被首次证实为Decursin直接作用靶点蛋白。Decursin通过抑制PKCδ磷酸化,进而阻断下游引发炎症反应和脂质吸收相关蛋白表达的信号通路(如p38和NF-κB通路)。
这项研究成功地将传统中药的活性成分与尖端的纳米生物技术相结合,开发出的ALD@EM纳米递送系统,不仅巧妙地克服了Decursin等天然药物的应用瓶颈,更是开创性地利用了疾病自身的病理生理特点来实现药物的精准靶向递送。
来源:附属医院
编辑:张懿淼 责任编辑:李哲